Introducción
La leucemia constituye el trastorno oncológico más frecuente en la infancia y se caracteriza por una alteración en la médula ósea que provoca una producción excesiva de células inmaduras denominadas blastos. Estas células, en lugar de proliferar y diferenciarse de manera normal, presentan un fallo en la diferenciación y se reproducen de forma incontrolada. Como consecuencia, se generan leucocitos no funcionales, lo que incrementa la susceptibilidad a infecciones. Además, la infiltración medular ocasiona una disminución en la producción de eritrocitos y trombocitos, lo que contribuye a la aparición de anemia y alteraciones hemorrágicas. ¹
Las leucemias se clasifican en agudas y crónicas, y según el tipo celular afectado, en linfoblásticas o mieloblásticas. Las leucemias linfoblásticas derivan de linfocitos B o T, mientras que las mieloblásticas se originan a partir de precursores de glóbulos rojos, neutrófilos, basófilos, eosinófilos y plaquetas. (2,3)
La leucemia linfoblástica aguda (LLA) es la neoplasia maligna más común en la población pediátrica, representando entre el 23 % y el 50 % de todos los cánceres en este grupo etario y aproximadamente el 80 % de las leucemias infantiles. Su incidencia es mayor en varones y se presenta con mayor frecuencia entre los 2 y 5 años de edad.
Manifestaciones bucales en LLA
Los pacientes pediátricos con LLA pueden presentar complicaciones orales tanto por la enfermedad como por los efectos adversos del tratamiento inmunosupresor y/o la radioterapia en cabeza y cuello. Cualquier fuente existente o potencial de infección oral o dental, así como traumatismos en tejidos blandos, puede comprometer el tratamiento médico y aumentar la morbilidad y mortalidad.
La higiene bucal deficiente y la acumulación de biofilm favorecen la inflamación y la hemorragia gingival espontánea, signo frecuente en estos pacientes, atribuible a trombocitopenia, neutropenia, alteración de la función granulocítica o infiltración leucémica directa. Las mucosas orales suelen presentar palidez secundaria a anemia, además de equimosis y petequias relacionadas con trombocitopenia.(4,5)
Recomendaciones para el tratamiento dental
La American Academy of Pediatric Dentistry (AAPD), en su revisión de 2022, recomienda que todos los pacientes sometidos a tratamiento inmunosupresor y/o radioterapia en cabeza y cuello reciban un examen bucal previo al inicio de la terapia, con el fin de identificar focos potenciales de infección que puedan complicar el manejo médico.(6)
Cuidados bucodentales antes del tratamiento inmunosupresor o radioterapia
- Identificar y estabilizar o eliminar focos de infección e irritantes locales sin retrasar el inicio del tratamiento ni inducir complicaciones.
- Comunicar al equipo médico el estado bucodental del paciente, el plan y el calendario de tratamiento.
- Educar al paciente y a sus cuidadores sobre la importancia del cuidado oral antes, durante y después del tratamiento, así como informar sobre los posibles efectos secundarios y secuelas a largo plazo.(7)
Cuidados durante la terapia inmunosupresora o radioterapia
- Conocer el estado hematológico del paciente y los riesgos asociados, principalmente bacteriemia y hemorragia, en coordinación con el oncólogo para determinar la necesidad de profilaxis antibiótica.
Parámetros para profilaxis antibiótica según recuento absoluto de neutrófilos:
- 2.000/mm³: no se requiere profilaxis.
- 1.000–2.000/mm³: decisión clínica según estado general y tipo de procedimiento.
- < 1.000/mm³: aplazar atención electiva.
Recomendaciones hematológicas para procedimientos odontológicos:
- Tratamientos electivos solo si neutrófilos > 1.000/mm³ y plaquetas > 60.000/mm³.
- Procedimientos urgentes para eliminar infecciones pueden realizarse en cualquier estado hematológico, coordinando con oncología. Considerar transfusión plaquetaria si < 100.000/mm³.
- Preferir pulpotomía/pulpectomía sobre extracción si no hay afección perirradicular. Extraer dientes con infección aguda/crónica o pronóstico dudoso, idealmente 5–7 días antes de quimioterapia/radioterapia.
Retirar aparatos de ortodoncia y prótesis removibles.
Las complicaciones orales más frecuentes incluyen mucositis, candidiasis, periodontitis, gingivitis y xerostomía inducida por quimioterapia. (8,9,10)
Cuidados posoperatorios
- Reforzar la importancia del cuidado bucodental de por vida.
- Abordar problemas dentales derivados de efectos tardíos del tratamiento inmunosupresor o radioterapia.(11)
Caso clínico
Se presenta el caso de una paciente de sexo femenino de 8 años de edad, segunda gestación, nacida mediante parto eutócico a las 39 semanas de gestación. El embarazo transcurrió sin complicaciones, aunque con control prenatal insuficiente. La paciente cuenta con diagnóstico confirmado de leucemia linfoblástica aguda (LLA) de células B y fue remitida desde una institución pública para valoración y tratamiento odontológico. Al momento de su atención, cursaba la fase de mantenimiento del protocolo de quimioterapia, clasificada como de riesgo estándar, recibiendo una sesión semanal indicada por el servicio de oncología pediátrica.
En la evaluación intraoral se identificó dentición mixta, presencia generalizada de biofilm y lesiones cariosas clasificadas como ICDAS 3 en los órganos dentarios 55, 74, 75 y 85, así como ICDAS 5 en los órganos 54 y 84. Se observó persistencia del órgano dentario 61. En la región correspondiente al órgano 64 se evidenció una lesión nodular, exofítica, de superficie lisa, color violáceo, consistencia fluctuante y bordes definidos, de aproximadamente 0,5 cm y asintomática, cuyo diagnóstico clínico fue compatible con un quiste de erupción (Figura 1).
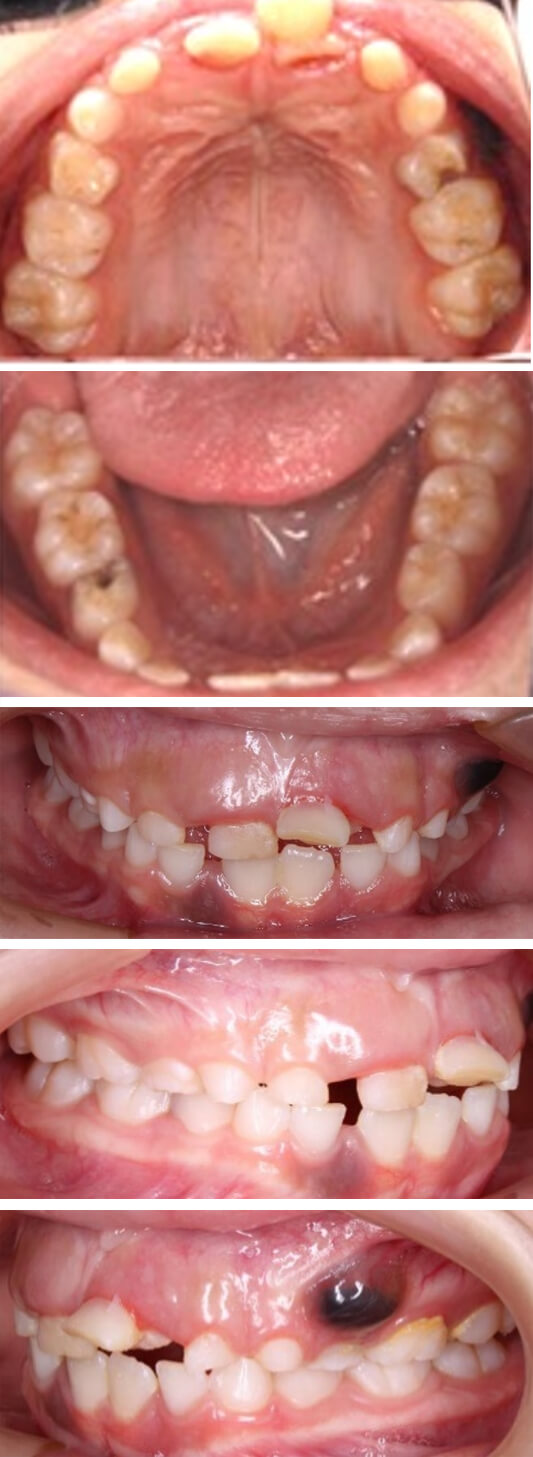
Figura 1
Se realizó interconsulta con el servicio de oncología, el cual indicó suspender la quimioterapia una semana previa al procedimiento odontológico programado para la extracción de las piezas afectadas. La paciente acudió con estudios hematológicos recientes (Figura 2) y se instauró profilaxis antibiótica consistente en amoxicilina 2 g vía oral, administrada 30 minutos antes del tratamiento.
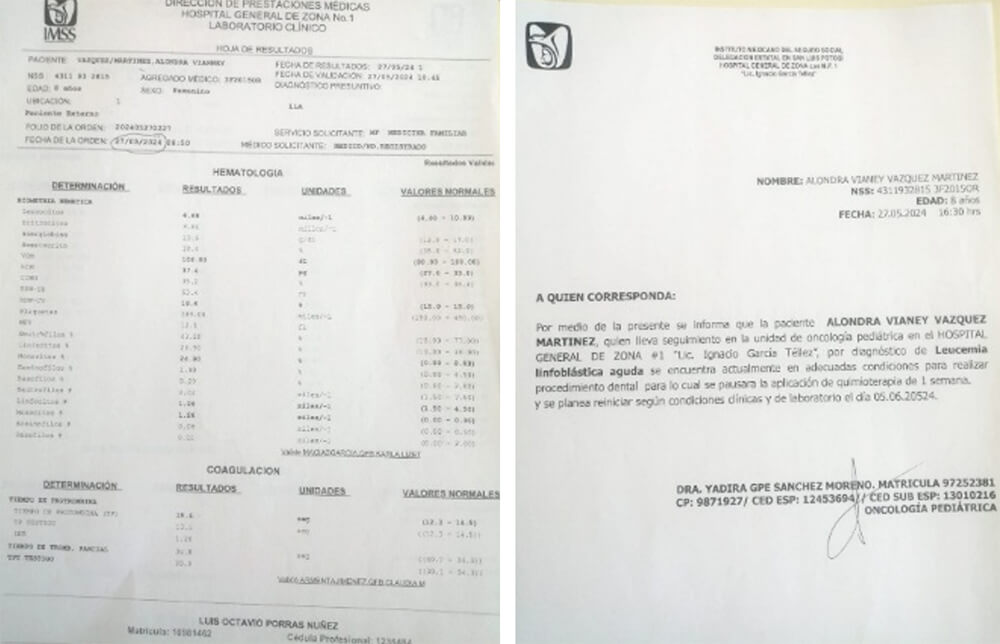
Figura 2
Bajo anestesia local infiltrativa con articaína al 3%, se realizaron las extracciones de los órganos dentarios 61, 64 y 84 sin complicaciones y con adecuada hemostasia. Se proporcionaron indicaciones posoperatorias a la madre y se programó revisión una semana después para valorar la evolución clínica (Figura 3).
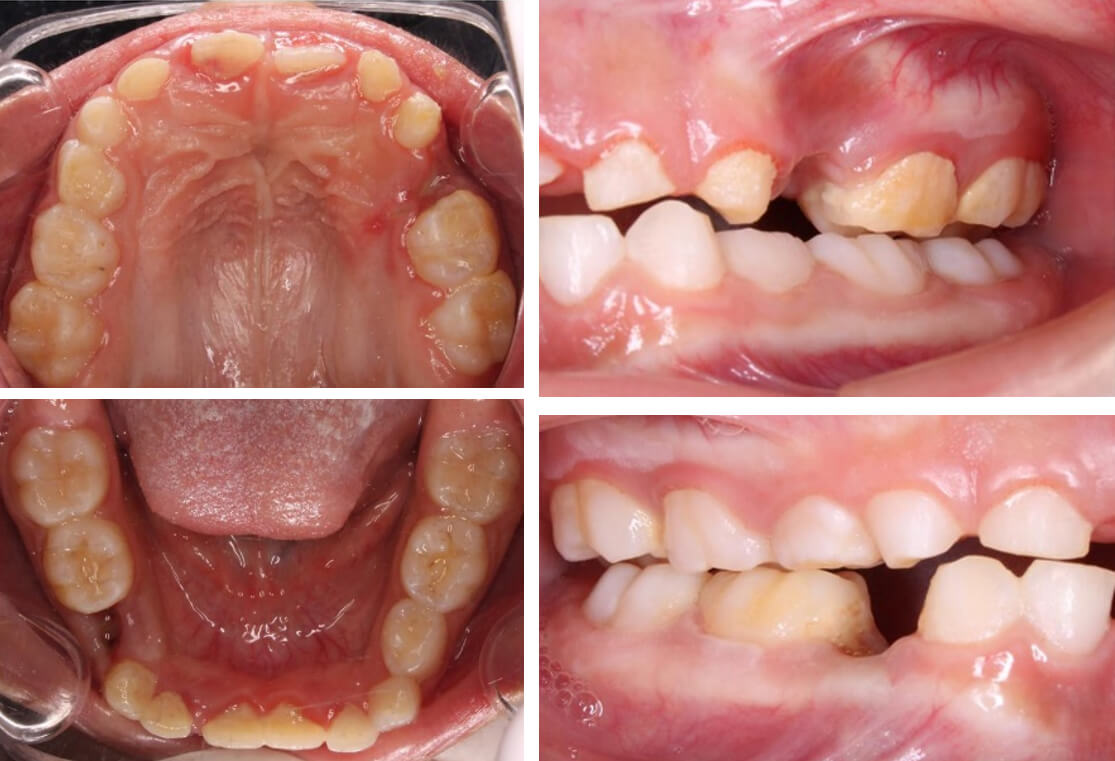
Figura 3
Discusión
El manejo odontológico en pacientes pediátricos con leucemia linfoblástica aguda (LLA) representa un desafío clínico debido a las alteraciones hematológicas y la inmunosupresión inducida por la quimioterapia. En este caso, la paciente se encontraba en fase de mantenimiento con riesgo estándar, lo que permitió planificar procedimientos dentales bajo estricta coordinación con el equipo de oncología pediátrica.
La presencia de biofilm generalizado y lesiones cariosas múltiples refleja la dificultad para mantener una adecuada higiene oral durante el tratamiento oncológico, situación ampliamente documentada en la literatura. Estas condiciones incrementan el riesgo de infecciones sistémicas, por lo que la eliminación de focos infecciosos es prioritaria antes de continuar la terapia inmunosupresora. La decisión de suspender la quimioterapia una semana antes del procedimiento y la administración de profilaxis antibiótica se alinean con las recomendaciones internacionales que sugieren evaluar parámetros hematológicos y aplicar medidas preventivas para reducir el riesgo de bacteriemia y hemorragia.(12)
El hallazgo de un quiste de erupción en el órgano dentario 64, ilustra la importancia de la vigilancia estomatológica en pacientes con LLA, ya que lesiones aparentemente simples pueden complicarse en un contexto de inmunosupresión. La intervención conservadora y la planificación adecuada contribuyen a evitar complicaciones mayores.
Este caso enfatiza la necesidad de un enfoque interdisciplinario, donde el odontopediatra desempeña un papel esencial en la prevención y manejo de complicaciones orales, asegurando la continuidad del tratamiento oncológico y mejorando la calidad de vida del paciente.
Los hallazgos presentan una revisión del estado actual del conocimiento y de las guías clínicas en el manejo bucodental de pacientes con leucemia linfoblástica aguda (LLA). Las manifestaciones orales tales como mucositis, gingivitis, candidiasis, petequias y xerostomía se asocian tanto a la patología hematológica subyacente como a los tratamientos (quimioterapia, radioterapia e inmunoterapias). Estas alteraciones pueden comprometer el tratamiento oncológico al elevar morbilidad y prolongar la hospitalización.(13.14)
Las guías de la AAPD (2022) insisten en la importancia de un examen bucal pretratamiento para eliminar focos infecciosos y estabilizar la cavidad oral, estableciendo una base para prevenir complicaciones más graves durante la terapia. Su inclusión en equipo multidisciplinario se refuerza en la literatura como esencial para una atención integral.
El ajuste de los tratamientos dentales según recuentos hematológicos es clave. La evidencia respalda:
- Neutrófilos >1 000/mm³ para atención electiva.
- Plaquetas >60 000/mm³ antes de procedimientos invasivos, con transfusiones antes si son <100 000/mm³ para urgencias.(15)
Conclusiones
- Las manifestaciones orales en niños con LLA son frecuentes y multifactoriales, elevando el riesgo de complicaciones sistémicas si no se abordadas adecuadamente.
- Una evaluación dental previa al inicio de quimioterapia o radioterapia es fundamental para impedir infecciones orales que puedan retrasar o complicar el tratamiento oncológico.
- Se deben aplicar protocolos de manejo basados en recuentos hematológicos:
Neutrófilos >1 000/mm³ para tratamientos electivos.
Plaquetas >60 000/mm³, con transfusión si <100 000/mm³ en urgencias.
Preferencia por tratamientos conservadores como pulpotomía frente a extracciones.
- Los odontopediatras deben integrarse al equipo oncohematológico, reforzando la coordinación para una atención segura y eficiente.
- Es prioritaria la educación continua del paciente y cuidadores para mantener una higiene bucal óptima durante todo el proceso terapéutico.
- Este caso confirma la relevancia del odontopediatra como parte del equipo multidisciplinario en el tratamiento integral del paciente oncológico pediátrico
Agradecimientos
A los docentes de los departamentos de Oncología Pediátrica y Cirugía Maxilofacial del Hospital Central “Ignacio Morones Prieto” por su valioso apoyo clínico y docente.
Referencias
- Tara H, Saavedra G. Manejo odontológico del paciente pediátrico con leucemia linfoblástica aguda. Gaceta dental, 2015; 274: 156-166.
- Tiol-Carrillo A, Enzaldo-de la Cruz P. Leucemia aguda linfoblástica Pre-B. Informe de un caso y revisión de la literatura Revista Odontológica Mexicana. 2017; 21 (1) 54-60.
- Aster JC. Enfermedades de los leucocitos, los ganglios linfáticos, el bazo y el timo. Patología estructural y funcional. Ed. Madrid, España: 2005, pp. 670-680.
- Parra JJ, Alvarado MC, Monsalve P, Costa ALF, Montesinos GA, Parra PA. Oral health in children with acute lymphoblastic leukaemia: before and after chemotherapy treatment. European Archives of Paediatric Dentistry. 2020;21(1):12936 https://pubmed.ncbi.nlm.nih.gov/31214964/
- American Academy of Pediatric Dentistry. Dental management of pediatric patients receiving immunosuppressive therapy and/or head and neck radiation. Manual of Pediatric Dentistry. American Academy of Pediatric Dentistry; 2023:549-58.
- Velten DB, Zandonade E, Monteiro de Barros Miotto MH. Prevalence of oral manifestations in children and adolescents with cancer submitted to chemotherapy. BMC Oral Health 2017; 17(1):49.
- Hong CH, Da Fonseca M. Considerations in the pediatric population with cancer. Dent Clin North Am 2008; 52 (1):155-81.
- Da Fonseca M. The Handbook of Pediatric Dentistry. 5th ed. Chicago, Ill. American Academy of Pediatric Dentistry; 2018:361-9.
- Levi LE, Lalla RV. Dental treatment planning for the patient with oral cancer. Dent Clin North Am 2018; 62 (1)121-30.
- Wang Y, Zeng X, Yang X, Que J, Du Q, Zhang Q, et al. Oral Health, Caries Risk Profiles, and Oral Microbiome of Pediatric Patients with Leukemia Submitted to Chemotherapy.BioMed Research International 2021.16; 2021: 1–11.
- Elad S, Raber-Durlacher JE, Brennan MT, et al. Basic oral care for hematology-oncology patients and hematopoietic stem cell transplantation recipients: A position paper from the joint task force of the Multinational Association of Supportive Care in Cancer/International Society of Oral Oncology (MASCC/ISOO) and the European Society for Blood and Marrow Transplantation (EBMT). Support Care Cancer 2015; 23(1):223-36.
- American Academy of Pediatric Dentistry. Guideline on Dental Management of Pediatric Patients Receiving Chemotherapy, Hematopoietic Cell Transplantation, and/or Radiation Therapy. The Reference Manual of Pediatric Dentistry; 2022:453–461.
- Bastos Silveira, Bruna et al. Oral manifestations in pediatric patients with leukemia. The Journal of the American Dental Association, Volume 155, Issue 10, 858 - 870.e30
- Subramaniam P, Babu KG, Nagarathna J. Oral manifestations in acute lymphoblastic leukemic children under chemotherapy. J Clin Pediatr Dent. 2008;32(4):319‑324.
- Zimmermann C, Meurer MI, Grando LJ, et al. Dental treatment in patients with leukemia. J Oncol. 2015; 25: 1-14.